СЕЛЛСЕПТ 250МГ. №100 КАПС. /ХОФФМАНН/
Персональный запрос
Спасибо за обращение!
Наш специалист скоро свяжется с Вами
Регистрационный номер
П N015393/01
Торговое наименование
Селлсепт®
Международное непатентованное название или группировочное название
Микофенолата мофетил
Лекарственная форма
Капсулы
Состав
Одна капсула содержит:
действующее вещество: микофенолата мофетил – 250 мг;
вспомогательные вещества: прежелатинизированный кукурузный крахмал – 29.76 мг, кроскармеллоза
натрия – 11.90 мг, повидон (К-90) – 5.95 мг, магния стеарат – 4.50 мг;
оболочка:
корпус - желатин, титана диоксид (Е171), краситель железа оксид красный
(Е172), краситель железа оксид желтый (Е172); крышечка – желатин,
титана диоксид (Е171), краситель индигокармин (Е132);
чернила для нанесения надписи на капсулу: шеллак, краситель железа оксид черный (Е172), калия гидроксид.
Описание
Твердые
желатиновые капсулы № 1, состоящие из непрозрачного корпуса
светло-коричневого цвета и непрозрачной крышечки светло-голубого цвета.
На корпусе имеется надпись «Roche» черного цвета, на крышечке –
«CellCept 250» черного цвета; содержимое капсул – мелкий гранулированный
порошок, частично скомковавшийся, от белого до почти белого цвета.
Фармакотерапевтическая группа
Иммунодепрессивное средство
Код АТХ
[L04AA06]
Фармакологические свойства
Иммунодепрессант, ингибитор инозинмонофосфатдегидрогеназы
Микофенолата
мофетил (ММФ) представляет собой 2-морфолиноэтиловый эфир микофеноловой
кислоты (МФК). МФК - мощный селективный неконкурентный и обратимый
ингибитор инозинмонофосфатдегидрогеназы (ИМФДГ), который подавляет
синтез гуанозиновых нуклеотидов de novo. Механизм, путем которого МФК
подавляет ферментную активность ИМФДГ, по-видимому, связан с тем, что
МФК структурно имитирует как кофактор никотинамиддинуклеотидфосфата, так
и катализирующую молекулу воды. Это препятствует окислению ИМФ в
ксантозо-5-монофосфат – важнейший этап биосинтеза гуанозиновых
нуклеотидов de novo. МФК оказывает более выраженное цитостатическое
действие на лимфоциты, чем на другие клетки, поскольку пролиферация Т- и
В-лимфоцитов очень сильно зависит от синтеза пуринов de novo, в то
время как клетки других типов могут переходить на обходные пути
метаболизма.
Эффективность
В
клинических исследованиях по профилактике отторжения после пересадки
почки, сердца и печени Селлсепт® применяли в комбинации со следующими
препаратами: иммуноглобулином антитимоцитарным, ОКТ3 (ортоклон мышиных
моноклональных антител), циклоспорином и глюкокортикостероидами.
Профилактика отторжения трансплантатов
Взрослые
Безопасность
и эффективность препарата Селлсепт® в комбинации с
глюкокортикостероидами и циклоспорином оценивались у больных после
трансплантации почки, сердца и печени.
Дети
Безопасность,
фармакокинетика и эффективность препарата Селлсепт® в комбинации с
глюкокортикостероидами и циклоспорином у детей после трансплантации
почки оценивались в исследовании при участии 100 детей в возрасте от 3
месяцев до 18 лет.
Трансплантация почки
Взрослые
В
комбинации с глюкокортикостероидами и циклоспорином Селлсепт®
статистически достоверно снижал частоту развития неэффективности терапии
в первые 6 месяцев после трансплантации и гистологически доказанного
отторжения в ходе терапии, в дозе 2 г/сутки снижает кумулятивную частоту
гибели трансплантата и летальности за 12 месяцев после трансплантации
почки, но в дозе 3 г в сутки увеличивает частоту преждевременного
выбывания из исследования по любой причине.
Дети
У детей после
трансплантации почки во всех возрастных группах прием препарата
Селлсепт®(порошок для приготовления суспензии) осуществлялся в дозах 600
мг/м2 два раза в день (до 1 г два раза в день).
Общая частота
случаев гистологически доказанного отторжения к 6 месяцу
посттрансплантационного периода была сравнима со значениями данного
показателя у взрослых и была сходной в различных возрастных группах.
Суммарная частота гибели трансплантата (5%) и летальности (2%) за 12
месяцев после трансплантации была сравнима со значениями, наблюдавшимися
у взрослых, перенесших трансплантацию почки.
Трансплантация сердца
Отторжение
Различий
в частоте гистологически доказанного отторжения, приведшего к нарушению
гемодинамики, в группах препарата Селлсепт® и азатиоприна не было.
Выживаемость
По показателю летальности и повторных трансплантаций при пересадке сердца ММФ превосходит азатиоприн.
Трансплантация печени
Препарат
Селлсепт® в комбинации с глюкокортикостероидами и циклоспорином более
эффективно, чем азатиоприн, предотвращал острое отторжение и обеспечивал
такую же выживаемость, как азатиоприн.
Доклинические данные по безопасности
В
дозах, в 2-3 раза превышающих терапевтические при пересадке почки и в
1.3-2 раза – по сравнению с таковым у пациентов после пересадки сердца,
ММФ не стимулировал образование опухолей и не влиял на фертильность
самцов крыс.
Два теста на генотоксичность указали на то, что в дозах, оказывающих серьезный токсический эффект, ММФ потенциально способен вызывать хромосомную нестабильность. В других тестах на генотоксичность наличие у препарата мутагенной активности не было выявлено.
В экспериментах по фертильности и репродуктивности самок крыс пероральный прием препарата вызывал пороки развития (в том числе анофтальмию, агнатию и гидроцефалию) в первом поколении потомства без какого-либо токсического действия на мать. В последующих поколениях потомства влияния на фертильность и репродуктивность не отмечалось.
В исследованиях тератогенности у крыс отмечалась резорбция плодов и врожденные пороки развития у потомства (включая анофтальмию, агнатию и гидроцефалию у крыс и пороки развития сердечно-сосудистой системы, почек, эктопия сердца и почек, диафрагмальные и пупочные грыжи у потомства кроликов) без признаков токсического действия на мать.
В токсикологических исследованиях ММФ на животных основные поражения локализовались в кроветворных и лимфоидных органах и возникали при таком уровне системной экспозиции препарата, который эквивалентен или меньше уровня экспозиции при приеме клинической дозы 2 г в сутки, рекомендованной больным после пересадки почки. Профиль неклинической токсичности ММФ совпадает с нежелательными явлениями, отмеченными в клинических исследованиях у человека, которые позволили получить данные по безопасности, более значимые для популяции пациентов (см. раздел «Побочное действие»).
Фармакокинетика
Фармакокинетические
характеристики ММФ изучались у пациентов, перенесших пересадку почки,
сердца и печени. В целом у больных после пересадки почки и сердца
фармакокинетический профиль МФК одинаков. В раннем
посттрансплантационном периоде у пациентов, перенесших пересадку печени и
получающих ММФ в дозе 1.5 г, концентрации МФК такие же, как у больных
после пересадки почки, получающих ММФ в дозе 1 г.
Всасывание
После
перорального приема происходит быстрое и полное всасывание и полный
пресистемный метаболизм ММФ с образованием активного метаболита – МФК.
Биодоступность ММФ при пероральном приеме, в соответствии с величиной
площади под кривой «концентрация – время» (AUCМФК), составляет, в
среднем, 94% от таковой при его внутривенном введении. После
перорального приема концентрации ММФ в плазме не определяются (ниже
порога определения - 0.4 мкг/мл).
В раннем посттрансплантационном периоде (до 40 дней после пересадки почки, сердца или печени) средние величины AUCМФК были примерно на 30% ниже, а максимальные концентрации – примерно на 40% ниже, чем в позднем посттрансплантационном периоде (3-6 месяцев после пересадки). Прием пищи не влияет на степень всасывания ММФ (AUCМФК) при его применении по 1.5 г два раза в сутки у больных после трансплантации почки. Однако максимальная концентрация МФК при приеме препарата во время еды снижается на 40%.
При исследовании биоэквивалентности двух пероральных форм выпуска ММФ было показано, что две таблетки по 500 мг эквивалентны четырем капсулам по 250 мг.
Распределение
Как
правило, примерно через 6-12 часов после приема препарата наблюдается
вторичное повышение концентрации МФК в плазме, что свидетельствует о
печеночно-кишечной рециркуляции препарата. При одновременном применении
колестирамина AUCМФК снижается примерно на 40%, что свидетельствует о
прерывании печеночно-кишечной рециркуляции.
В клинически значимых концентрациях МФК на 97% связывается с альбумином плазмы.
Метаболизм
МФК
метаболизируется, в основном, под действием глюкуронилтрансферазы
(изоформа гена UGT1A9) с образованием фармакологически неактивного
фенольного глюкуронида МФК (МФКГ). In vivo МФКГ обратно превращается в
свободную МФК в ходе печеночно-кишечной рециркуляции с образованием
ацилглюкуронида, который обладает фармакологической активностью и
возможно является причиной некоторых побочных эффектов МФК (диарея,
лейкопения).
Выведение
После
перорального приема радиоактивно меченного ММФ 93% полученной дозы
выводится с мочой, а 6% - с калом. Большая часть (около 87%) введенной
дозы выводится с мочой в виде МФКГ. Незначительные количества препарата
(<1% дозы) выводятся с мочой в виде МФК.
Клинически определяемые концентрации МФК и МФКГ не удаляются путем гемодиализа. Однако при более высоких концентрациях МФКГ (>100 мкг/мл) некоторая его часть может быть удалена. Секвестранты желчных кислот типа колестирамина снижают AUCМФК, прерывая печеночно-кишечную рециркуляцию.
Распределение МФК зависит от нескольких транспортеров: транспортный полипептид органических анионов (ТПОА) и белок, ассоциированный с множественной лекарственной устойчивостью -2 (БАМЛУ-2). Изоформы ТПОА, БАМЛУ-2, а также белок резистентности рака молочной железы (БРРМ) являются транспортерами, ассоциированными с экскрецией глюкуронида через желчь. Белок множественной лекарственной резистентности -1 также может принимать участие в переносе МФК, но его участие ограничено процессом всасывания. МФК и его метаболиты потенциально могут вступать в реакцию с транспортерами органических анионов в почках.
Фармакокинетика в особых клинических случаях
В исследовании с разовым приемом препарата у больных с тяжелой хронической почечной недостаточностью (скорость клубочковой фильтрации <25 мл/мин/1.73 м2) AUCМФК была на
28-75% больше, чем у здоровых добровольцев и больных с менее выраженным
поражением почек. После приема разовой дозы AUCМФКГ в 3-6 раз больше у
больных с тяжелой почечной недостаточностью, чем у здоровых добровольцев
и пациентов с умеренным поражением почек, что согласуется с данными о
почечном выведении МФКГ.
Исследований по многократному введению ММФ при тяжелой хронической почечной недостаточности не проводилось.
У больных с задержкой функции почечного трансплантата после пересадки среднее значение AUC0-12для МФК сравнимо с таковым у больных, у которых трансплантат начинал функционировать после пересадки без задержки. У пациентов с задержкой функции почечного трансплантата может наблюдаться транзиторное увеличение свободной фракции и концентрации МФК в плазме крови. Вероятно, необходимости в коррекции дозы препарата Селлсепт® у этих пациентов нет (см. раздел «Дозирование в особых случаях»). Среднее значение AUC0-12 для МФКГ в плазме было в 2-3 раза больше, чем у пациентов, у которых трансплантат начинал функционировать после пересадки без задержки.
У пациентов с первично нефункционирующим трансплантатом после трансплантации почки наблюдалось увеличение концентрации МФКГ в плазме крови; кумуляция МФК, если и отмечалась, то в гораздо меньшей степени по сравнению с МФКГ.
Больные с поражением печени. У добровольцев с алкогольным циррозом печени после перорального приема ММФ не выявлено изменений в фармакокинетике МФК и МФКГ. Влияние печеночной патологии на этот процесс, вероятно, зависит от конкретного заболевания. В случае болезни печени с преобладанием поражения желчевыводящих путей (например, первичный билиарный цирроз) изменения в фармакокинетике МФК и МФКГ нельзя исключить.
У пациентов детского возраста (≤18 лет), перенесших пересадку почки, после перорального приема ММФ в дозе 600 мг/м2 два раза в сутки (максимально до 1 г два раза в сутки) AUC для МФК сравнима с таковой у взрослых пациентов после пересадки почки, получающих препарат в дозе 1 г два раза в сутки, в раннем и позднем посттрансплантационном периоде. Значения AUC для МФК не различались между возрастными группами в раннем и позднем трансплантационном периоде.
У больных пожилого и старческого возраста (³65 лет) фармакокинетика не изучалась.
Показания к применению
Селлсепт® применяют в виде комбинированной терапии с циклоспорином и глюкокортикостероидами.
Взрослые и дети с площадью поверхности тела >1.25 м2 (примерный возраст старше 12 лет):
- профилактика острого отторжения трансплантата у больных после аллогенной пересадки почки.
Взрослые:
- профилактика острого отторжения трансплантата у больных после аллогенной пересадки сердца;
- профилактика острого отторжения трансплантата у больных после аллогенной пересадки печени.
Противопоказания
Повышенная индивидуальная чувствительность к ММФ, МФК и другим компонентам препарата.
Дефицит гипоксантингуанинфосфорибозилтрансферазы (редкое генетическое заболевание, обусловленное наследственным дефицитом гипоксантингуанинфосфорибозилтрансферазы - синдромы Леша-Найена и Келли-Зигмиллера).
Одновременный прием с азатиоприном (оба препарата угнетают костный мозг, их одновременный прием не изучался).
Дети с площадью поверхности тела <1.25 м2 (примерный детский возраст до 12 лет).
Беременность (применение препарата Селлсепт® противопоказано во время беременности вследствие его мутагенного и тератогенного потенциала).
Женщины детородного потенциала, не использующие высокоэффективные методы контрацепции.
Период грудного вскармливания.
С осторожностью
Заболевания
желудочно-кишечного тракта (ЖКТ) (в фазе обострения), одновременный
прием ММФ с такролимусом, сиролимусом, с препаратами, влияющими на
печеночно-кишечную рециркуляцию.
Применение при беременности и в период грудного вскармливания
Применение
препарата Селлсепт® противопоказано во время беременности и у женщин
детородного потенциала, не использующих высокоэффективные методы
контрацепции.
Перед началом терапии пациентов с репродуктивным потенциалом, как мужчин, так и женщин, необходимо проинформировать о повышенном риске смерти плода и врожденных пороках развития; следует провести консультацию о мерах предотвращения беременности и ее планировании.
Перед началом терапии препаратом Селлсепт® у пациенток детородного потенциала должен быть получен отрицательный результат двух тестов на беременность при использовании метода анализа сыворотки или мочи с чувствительностью не менее 25 мМЕ/мл; второй тест должен быть проведен через 8-10 дней после первого теста и непосредственно до начала приема препарата Селлсепт®.
Повторные тесты на беременность должны проводиться во время стандартных визитов последующего наблюдения. Результаты всех тестов на беременность необходимо обсудить с пациенткой. Пациентки должны быть проинформированы, что в случае наступления беременности им необходимо незамедлительно проконсультироваться с лечащим врачом.
Вследствие мутагенного и тератогенного потенциала препарата Селлсепт® женщины детородного потенциала должны использовать два надежных метода контрацепции одновременно (поскольку потенциально возможно снижение концентрации гормонов при пероральном приеме контрацептивных препаратов на фоне терапии препаратом Селлсепт®), включая по меньшей мере один высокоэффективный метод, до начала терапии, во время терапии и в течение шести недель после прекращения терапии препаратом Селлсепт®, если воздержание от половой жизни невозможно. Ведущим активную половую жизнь мужчинам рекомендуется использовать презервативы во время лечения и в течение как минимум 90 дней после прекращения лечения.
Использовать презервативы должны как мужчины с нормальной репродуктивной функцией, так и мужчины после вазэктомии, поскольку риски, связанные с передачей семенной жидкости, также применимы к мужчинам, перенесшим вазэктомию. Кроме того, женщинам-партнершам пациентов-мужчин рекомендуется использовать высокоэффективные методы контрацепции во время лечения и в течение 90 дней после приема последней дозы препарата Селлсепт®.
При пострегистрационном применении у детей пациенток, получавших лечение ММФ в комбинации с другими иммуносупрессантами во время беременности, были выявлены врожденные пороки развития, включая множественные пороки развития.
Наиболее часто отмечались следующие пороки развития:
- пороки развития лица, такие как расщепленная губа, расщепленное небо, микрогнатия и гипертелоризм глазниц;
- аномалии развития уха (например, аномалия формы или отсутствие наружного/среднего уха) и глаза (например, колобома, микрофтальм);
- пороки развития пальцев (например, полидактилия, синдактилия, брахидактилия);
- аномалии сердца, такие как дефект межпредсердной и межжелудочковой перегородок;
- пороки развития пищевода (например, атрезия пищевода);
- пороки развития нервной системы (такие как незаращение дужек позвонков).
В медицинской литературе сообщалось о пороках развития у 23-27% живорожденных детей, подвергшихся воздействию микофенолата мофетила во время внутриутробного развития. Для сравнения, риск пороков развития у живорожденных детей составляет приблизительно 2% в общей популяции и приблизительно 4-5% у пациентов, перенесших трансплантацию солидных органов, получающих лечение другими иммуносупрессантами помимо микофенолата мофетила.
У пациенток, получавших микофенолата мофетил, выявлен повышенный риск самопроизвольного выкидыша, в основном в I триместре беременности.
По данным медицинской литературы риск у пациентов, получавших микофенолата мофетил, составил 45-49% в сравнении с частотой 12-33% у пациентов, получавших лечение другими иммуносупрессантами после трансплантации солидных органов.
Исследования на животных показали наличие репродуктивной токсичности.
Препарат Селлсепт® противопоказан в период грудного вскармливания в связи с возможностью серьезных нежелательных реакций у детей, находящихся на грудном вскармливании.
У крыс ММФ выделяется с молоком. Выделяется ли ММФ с женским молоком, неизвестно.
Способ применения и дозы
Внутрь.
Взрослые
Профилактика отторжения трансплантата почки
Прием
препарата необходимо начать в течение 72 часов после проведения
операции трансплантации. Больным с почечными трансплантатами
рекомендуется прием по 1 г два раза в сутки (суточная доза 2 г). Хотя в
клинических исследованиях было показано, что доза в 1.5 г два раза в
сутки (суточная доза 3 г) также является безопасной и эффективной, ее
преимущества в плане эффективности у больных после пересадки почки не
установлены. У больных, получавших 2 г ММФ в сутки, профиль безопасности
был в целом лучше, чем у получавших суточную дозу в 3 г.
Профилактика отторжения трансплантата сердца
Прием
препарата необходимо начать в течение 5 дней после проведения операции
трансплантации. Pекомендованный режим дозирования – по 1.5 г 2 раза в
сутки (суточная доза 3 г).
Профилактика отторжения трансплантата печени
Прием
препарата необходимо начать как можно раньше после проведения операции
трансплантации (в зависимости от возможности пациента переносить
препарат). Рекомендованный режим дозирования – по 1.5 г 2 раза в сутки
(суточная доза 3 г).
Дозирование в особых случаях
При нейтропении (абсолютное
число нейтрофилов <1300 в 1 мкл крови) необходимо прервать лечение
ММФ или уменьшить его дозу и тщательно наблюдать пациента (см. раздел
«Особые указания»).
У больных с тяжелой хронической почечной недостаточностью (скорость клубочковой фильтрации менее 25 мл/мин/1.73 м2) вне ближайшего посттрансплантационного периода следует избегать доз выше 1 г 2 раза в сутки. Данные по пациентам с тяжелой почечной недостаточностью, перенесшим пересадку сердца или печени, отсутствуют (см. раздел «Особые указания»).
Коррекции дозы больным с задержкой функции почечного трансплантата не требуется (см. раздел «Фармакокинетика в особых клинических случаях»).
Больным, перенесшим пересадку почки и имеющим тяжелое поражение паренхимы печени, коррекция дозы не требуется (см. раздел «Фармакокинетика в особых клинических случаях»). Данные по пациентам с тяжелым поражением паренхимы печени, перенесшим пересадку сердца, отсутствуют.
У больных пожилого и старческого возраста (³65 лет), перенесших пересадку почки, рекомендуемая доза равняется 1 г 2 раза в сутки, а после пересадки сердца или печени – 1.5 г 2 раза в сутки (см. раздел «Особые указания»).
Дети:
- профилактика отторжения трансплантата почки:
у пациентов детского возраста старше 12 лет, перенесших трансплантацию почки, при
площади поверхности 1.25-1.50 м² возможно применение капсул по 750 мг
два раза в сутки (суточная доза 1.5 г), при площади поверхности более
1.50 м² возможно применение капсул по 1 г два раза в сутки (суточная
доза 2 г);
- данные по безопасности и эффективности препарата у больных детского возраста после пересадки сердца или печени отсутствуют.
Передозировка
Данные
о передозировке ММФ были получены в клинических исследованиях и при
пострегистрационном применении. В большинстве случаев данных о
нежелательных явлениях не зарегистрировано. При передозировке
нежелательных явлений дополнительно к нижеописанным не выявлено.
Ожидается, что передозировка ММФ вероятно приведет к чрезмерной иммуносупрессии (как следствие этого к повышению чувствительности к инфекциям) и угнетению костного мозга (см. раздел «Особые указания»). В случае развития нейтропении прием препарата Селлсепт® должен быть прекращен или снижена доза препарата (см. раздел «Особые указания»). МФК нельзя удалить из организма методом гемодиализа. Однако, при высоких концентрациях МФКГ в плазме (>100 мкг/мл) небольшие его количества все-таки выводятся. Препараты, связывающие желчные кислоты, например, колестирамин, могут способствовать устранению МФК из организма, увеличивая его экскрецию.
Побочное действие
Профиль
побочных действий, связанных с применением иммунодепрессантов, часто
трудно установить из-за наличия основного заболевания и одновременного
применения многих других лекарственных средств.
Данные клинических исследований
Основными
побочными реакциями, связанными с применением ММФ в комбинации с
циклоспорином и глюкокортикостероидами для профилактики отторжения
почечного, сердечного или печеночного трансплантата, являются диарея,
лейкопения, сепсис и рвота; существуют также данные о повышении частоты
некоторых типов инфекций, например, оппортунистических (см. раздел
«Особые указания»).
Злокачественные новообразования
Как
и на фоне комбинированной иммуносупрессии вообще, так и при применении
ММФ, как компонента иммуносупрессивной схемы, имеется повышенный риск
развития лимфом и других злокачественных новообразований, особенно кожи
(см. раздел «Побочное действие»). В контролируемых клинических
исследованиях у больных, перенесших пересадку почки, сердца или печени и
наблюдавшихся не менее 1 года, лимфопролиферативные заболевания или
лимфомы развились у 0.4-1% больных, получавших ММФ (в дозах 2 или 3 г в
сутки) в комбинации с другими иммунодепрессантами. Рак кожи (исключая
меланому) отмечался у 1.6-3.2% больных, злокачественные новообразования
других типов – у 0.7-2.1% больных. Трехлетние данные по безопасности у
пациентов после пересадки почки или сердца не выявили каких-либо
неожиданных изменений в показателе заболеваемости злокачественных
новообразований, по сравнению с годичными показателями. После пересадки
печени больных наблюдали не менее 1 года, но меньше 3 лет.
Оппортунистические инфекции
Риск
оппортунистических инфекций повышен у всех посттрансплантационных
пациентов и возрастает с увеличением степени иммуносупрессии (см. раздел
«Особые указания»). В контролируемых клинических исследованиях при
применении ММФ (2 или 3 г в сутки) в комбинации с другими
иммунодепрессантами у больных, наблюдавшихся в течение 1 года после
пересадки почки (на дозе 2 г в сутки), сердца и печени, самыми частыми
инфекциями были кандидоз кожи и слизистых оболочек, цитомегаловирусная
(ЦМВ) инфекция: ЦМВ виремия/ЦМВ синдром (13.5%) и инфекция, вызванная
вирусом простого герпеса.
После пересадки почки сепсис (как правило, связанный с ЦМВ) чаще возникал у пациентов, получавших ММФ, чем у пациентов контрольной группы. У пациентов, получавших ММФ в дозе 3 г, частота случаев сепсиса была выше, чем у пациентов, получавших ММФ в дозе 2 г.
Дети (3 месяца – 18 лет)
Тип нежелательных реакций и частота их возникновения в клиническом исследовании при пероральном приеме 600 мг/м2 ММФ 2 раза в сутки у детей в возрасте от 3 месяцев до 18 лет (N=100)
практически не отличались от таковых у взрослых пациентов, получавших
препарат в дозе 1 г 2 раза в сутки. Однако, такие побочные реакции как
диарея, лейкопения, сепсис, инфекции, анемия встречались чаще (≥10%) у
детей, особенно в возрасте до 6 лет.
У больных пожилого и старческого возраста (³65 лет) при лечении ММФ в рамках комбинированной иммуносупрессивной терапии риск некоторых инфекций (включая тканевые инвазивные формы манифестной цитомегаловирусной инфекции), а также, возможно, желудочно-кишечных кровотечений и отека легких выше, чем у пациентов более молодого возраста (см. раздел «Особые указания»).
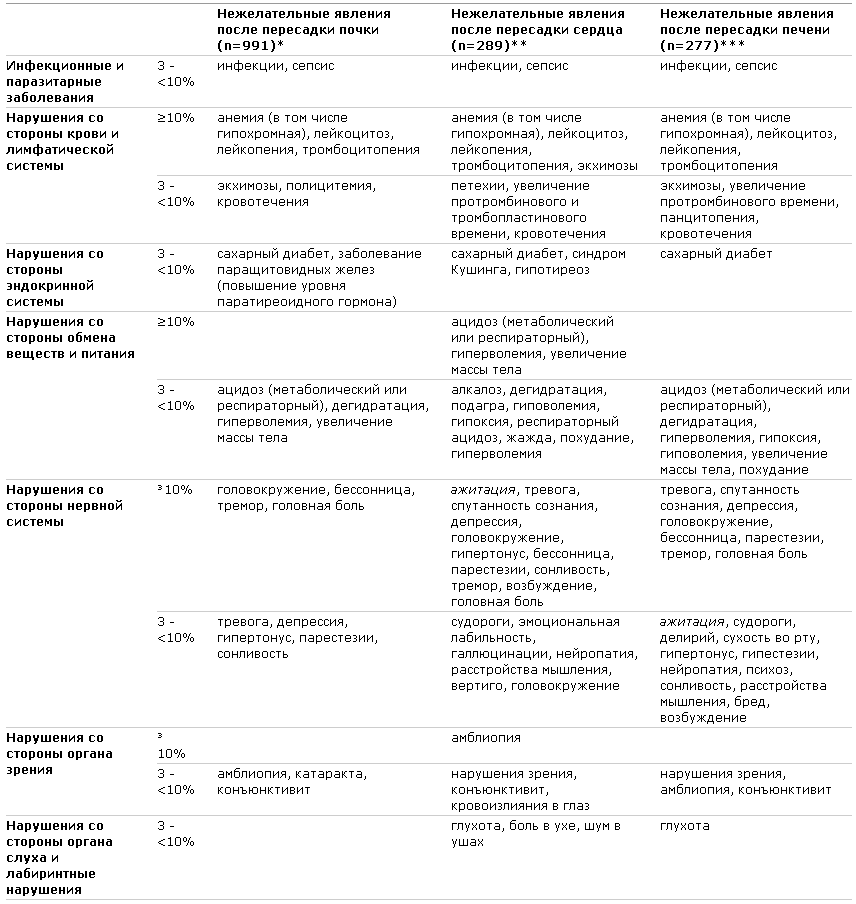
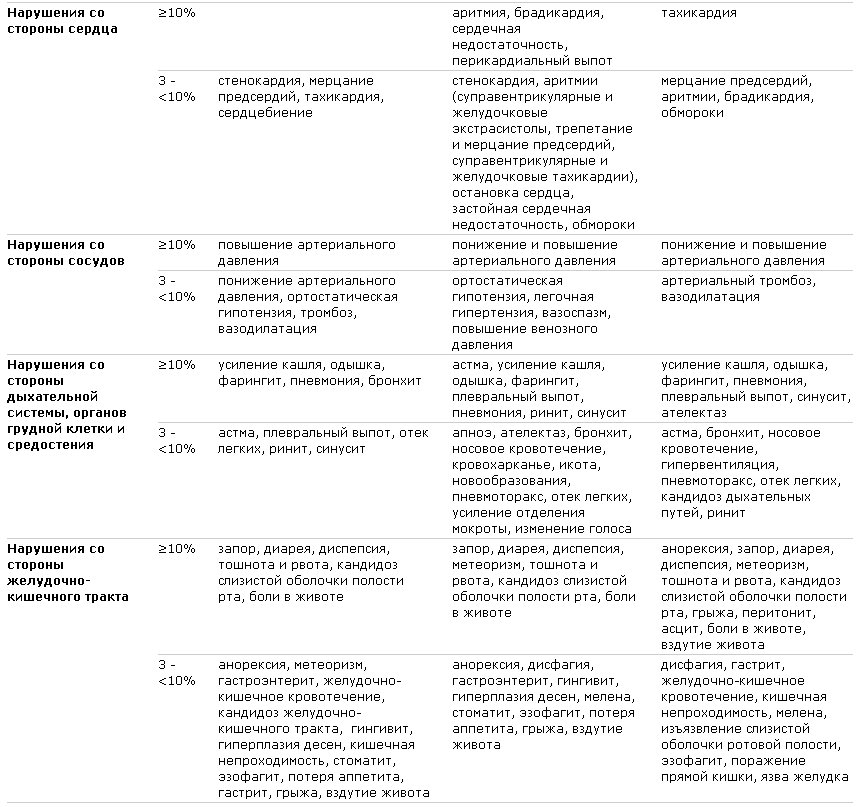
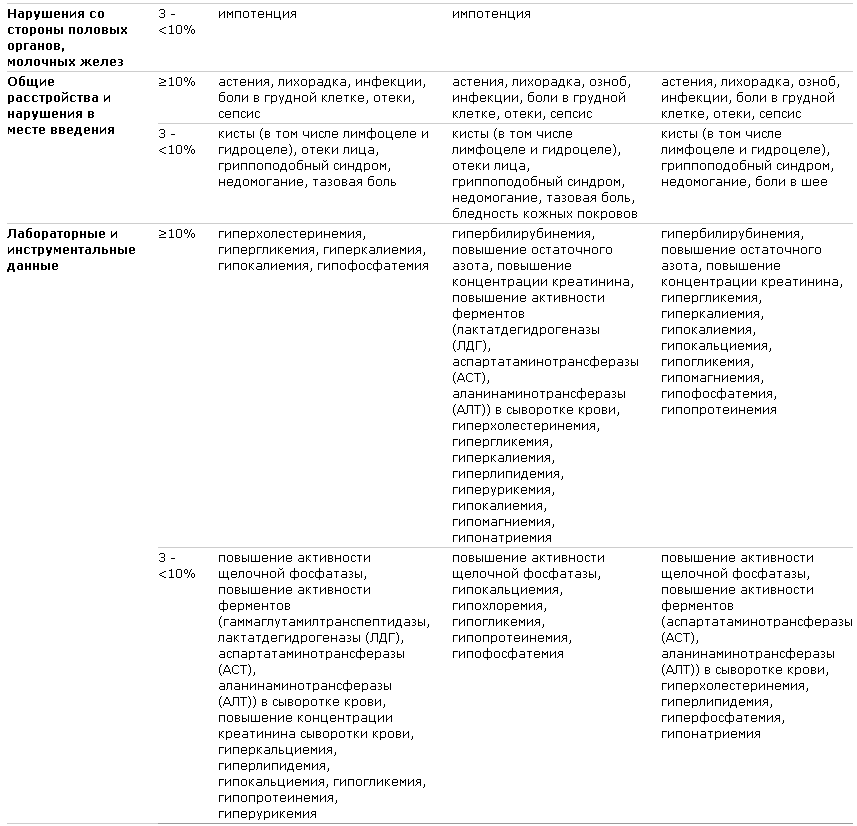
Нежелательные явления, отмеченные у ³10% и у 3-10% больных, получавших ММФ в комбинации с циклоспорином и глюкокортикостероидами в контролируемых исследованиях по профилактике отторжения почечного трансплантата (3 исследования, данные по суточной дозе 2 и 3 мг), в контролируемом исследовании по пересадке сердца и в контролируемом исследовании по пересадке печени.
В трех контролируемых исследованиях по профилактике отторжения почечного трансплантата профиль безопасности ММФ в суточной дозе 2 г был несколько лучше, чем в суточной дозе 3 г.
Пострегистрационное применение препарата
Инфекции:
отдельные случаи тяжелых, угрожающих жизни инфекций (менингита,
инфекционного эндокардита), повышение частоты некоторых инфекций типа
туберкулеза и атипичных микобактериальных инфекций.
Случаи прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ), иногда фатальные, наблюдались у пациентов, принимавших Селлсепт®. В сообщениях об этих случаях имеется информация о наличии у пациентов дополнительных факторов риска развития ПМЛ, включающих иммуносупрессивную терапию и ухудшение состояния иммунитета.
У пациентов, принимавших Селлсепт®, наблюдались случаи развития нефропатии, ассоциированной с BK-вирусом (BK virus - associated nephropathy). Данная инфекция может приводить к серьезным последствиям, иногда к гибели трансплантата почки.
Со стороны крови и иммунной системы: случаи развития парциальной красноклеточной аплазии (ПККА) и гипогаммаглобулинемии наблюдались у пациентов, принимавших Селлсепт® в комбинации с другими иммуносупрессивными препаратами.
Аномалии развития: в пострегистрационном периоде зарегистрированы случаи врожденных пороков развития у детей пациенток, принимавших Селлсепт® во время беременности в комбинации с другими иммунодепрессантами.
Беременность, послеродовые и перинатальные состояния: у пациенток, получавших микофенолата мофетил, зарегистрированы случаи самопроизвольного выкидыша, в основном в I триместре беременности.
Со стороны органов пищеварения: колит (иногда цитомегаловирусной этиологии), панкреатит, отдельные случаи атрофии кишечных ворсинок.
Другие нежелательные реакции, наблюдавшиеся при пострегистрационном применении препарата, не отличаются от нежелательных реакций, зарегистрированных в контролируемых клинических исследованиях.
Взаимодействие с другими лекарственными средствами
Ацикловир
При
одновременном применении ММФ и ацикловира наблюдались более высокие
концентрации МФКГ и ацикловира в плазме, чем при применении каждого
препарата отдельно. Поскольку плазменные концентрации МФКГ, как и
ацикловира, повышаются при почечной недостаточности, есть вероятность,
что эти два препарата конкурируют в отношении канальцевой секреции, что
может приводить к дальнейшему повышению концентрации обоих лекарственных
средств.
Антациды и ингибиторы протонного насоса (ИПН)
При совместном применении препарата Селлсепт® c
антацидами (алюминия и магния гидроксид) и с ингибиторами протонного
насоса (лансопразол и пантопразол) наблюдалось снижение концентрации
МФК. Однако значительная разница между частотами отторжения
трансплантата у пациентов, принимающих препарат Селлсепт® одновременно с препаратами ИПН и без таковых, отсутствовала. Данное
заключение теоретически распространяется и на антациды, так как при их
приеме одновременно с препаратом Селлсепт® концентрация МФК снижается в гораздо меньшей степени, чем при одновременном приеме препарата Селлсепт® с ИПН.
Колестирамин
После
применения разовой дозы ММФ 1.5 г у здоровых добровольцев,
предварительно принимавшим по 4 г колестирамина 3 раза в сутки на
протяжении 4 дней, наблюдалось уменьшение AUCМФК на 40%. Необходимо соблюдать осторожность при одновременном применении
ММФ и препаратов, влияющих на печеночно-кишечную рециркуляцию (см.
раздел «Особые указания»).
Циклоспорин
ММФ не влияет на фармакокинетику циклоспорина. Однако циклоспорин влияет на печеночно-кишечную рециркуляцию МФК, что может привести к увеличению AUCМФК примерно на 30% при прекращении приема циклоспорина у пациентов после трансплантации почек, получающих препарат Селлсепт® и циклоспорин (по сравнению с пациентами, получающими сиролимус или белатацепт с аналогичными дозами препарата Селлсепт®).
Напротив, при переходе пациентов с терапии циклоспорином на терапию
иммуносупрессантами, не влияющими на печеночно-кишечную рециркуляцию
МФК, следует ожидать изменение экспозиции МФК.
Телмисартан
Одновременное применение с препаратом Селлсепт® приводит к уменьшению концентрации МФК примерно на 30%. Телмисартан
оказывает влияние на выведение МФК путем увеличения экспрессии гамма
рецептора, активируемого пероксисомными пролифераторами, что в свою
очередь увеличивает экспрессию и активность гена UGT1A9. Не было
выявлено клинических проявлений лекарственного взаимодействия при
сравнении частоты отторжения трансплантата и профилей нежелательных
явлений у пациентов, получающих препарат Селлсепт® с или без сопутствующей терапии телмисартаном.
Ганцикловир
По
результатам исследования с однократным пероральным приемом
рекомендованных доз ММФ и внутривенным введением ганцикловира с учетом
известного влияния почечной недостаточности на фармакокинетику ММФ (см.
разделы «Фармакокинетика в особых клинических случаях» и «Особые
указания») и ганцикловира можно предположить, что одновременное
применение этих двух препаратов (конкурирующих в процессе канальцевой
секреции) приведет к повышению концентраций МФКГ и ганцикловира.
Существенного изменения фармакокинетики МФК не ожидается, поэтому
корректировать дозу ММФ не нужно. Если ММФ и ганцикловир (или его
пролекарства, например, валганцикловир) применяют у больных с почечной
недостаточностью, необходимо тщательно наблюдать больных.
Пероральные контрацептивы
В
исследовании при участии 18 женщин с псориазом при одновременном приеме
на протяжении 3 менструальных циклов препарата Селлсепт® (1 г 2 раза в сутки) с комбинированными пероральными контрацептивами,
содержащими этинилэстрадиол (0.02-0.04 мг) и левоноргестрел (0.05-0.2
мг), дезогестрел (0.15 мг) или гестоден (0.05-0.1 мг), не было выявлено
клинически значимого воздействия препарата Селлсепт® на концентрации прогестерона, лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ). Таким образом, Селлсепт® не оказывал влияния на подавление овуляции под действием пероральных
контрацептивов. Фармакокинетика пероральных контрацептивов не изменялась
в клинически значимой степени при совместном применении с препаратом
Селлсепт®.
Однако во время приема препарата Селлсепт® дополнительно к пероральным контрацептивам необходимо использовать и другие методы контрацепции (см. раздел «Применение при беременности и в период грудного вскармливания»).
Такролимус
При одновременном применении не выявлено влияния на AUC и максимальную концентрацию (Сmax)МФК у пациентов после пересадки печени и почек. У пациентов после трансплантации почек применение препарата Селлсепт® не влияло на концентрацию такролимуса. У больных со стабильным
печеночным трансплантатом AUC такролимуса после многократного приема ММФ
в дозе 1.5 г 2 раза в сутки возрастала примерно на 20%.
Сиролимус
У пациентов после трансплантации почек одновременный прием препарата Селлсепт® и циклоспорина приводил к уменьшению экспозиции МФК на 30-50% по
сравнению с пациентами, получающими комбинацию сиролимуса и препарата
Селлсепт®.
Рифампицин
После коррекции дозы отмечено уменьшение экспозиции МФК на 70% (AUC0-12)
у пациентов после одномоментной трансплантации сердца и легких,
рекомендуется контроль экспозиции МФК и коррекция дозы препарата
Селлсепт® для поддержания клинического эффекта при совместном применении.
Антибиотики, приводящие к гибели бактерий, продуцирующих β-глюкуронидазу в кишечнике (например, антибиотики из группы аминогликозидов, цефалоспоринов, фторхинолонов и пенициллинов), могут нарушать печеночно-кишечную рециркуляцию МФКГ/МФК, что в свою очередь может привести к снижению системной экспозиции МФК.
Доступна информация о следующих антибиотиках.
Ципрофлоксацин или амоксициллин в комбинации с клавулановой кислотой
У
пациентов после трансплантации почек в дни непосредственно после
перорального приема ципрофлоксацина или амоксициллина в комбинации с
клавулановой кислотой наблюдается снижение минимальной концентрации МФК
на 54%. При продолжении антибактериальной терапии данный эффект
снижается, а после прекращения терапии - исчезает. Клиническое значение
этого явления не известно, поскольку изменение минимальной концентрации
может неадекватно отражать изменение суммарной экспозиции МФК.
Норфлоксацин и метронидазол
Применение норфлоксацина в комбинации с метронидазолом снижает AUC0-48 МФК на 30% после однократного приема препарата Селлсепт®. При отдельном применении одного из этих антибиотиков такое влияние на системную экспозицию МФК отсутствует.
Триметоприм/сульфаметоксазол
При комбинированном применении с триметопримом/сульфаметоксазолом влияние на системную экспозицию МФК (AUC, Cmax) не отмечалось.
Другие взаимодействия
При одновременном применении пробенецида и ММФ обезьянами отмечалось увеличение AUC МФКГ в плазме в 3 раза.
Таким образом, другие лекарственные средства, подвергающиеся канальцевой
секреции, могут конкурировать с МФКГ, что приводит к увеличению
концентрации МФКГ или другого препарата в плазме, который также
подвергается канальцевой секреции.
Севеламер
Одновременное применение севеламера и МФК у взрослых и детей снижало Сmax и AUC0-12 МФК на 30% и 25%, соответственно. Севеламер и другие фосфатсвязывающие
препараты, не содержащие кальций, должны применяться через 2 часа после
приема препарата Селлсепт®, чтобы уменьшить влияние на всасывание МФК.
Живые ослабленные вакцины
Не
должны вводиться пациентам в состоянии иммунодепрессии.
Антителообразование в ответ на другие вакцины может быть снижено (см.
раздел «Особые указания»).
Особые указания
Новообразования
Как
и на фоне комбинированной иммуносупрессии вообще, так и при применении
ММФ как компонента иммуносупрессивной схемы, имеется повышенный риск
развития лимфом и других злокачественных новообразований, особенно кожи
(см. раздел «Побочное действие»). Этот риск, по-видимому, связан не с
применением какого-либо препарата как такового, а с интенсивностью и
продолжительностью иммуносупрессии.
Как и у всех больных с повышенным риском рака кожи, следует ограничить воздействие солнечных и ультрафиолетовых лучей ношением соответствующей закрытой одежды и использованием солнцезащитных кремов с высоким значением защитного фактора.
Инфекции
Чрезмерное
подавление иммунной системы может также повысить восприимчивость к
инфекциям, в том числе оппортунистическим, сепсису и другим инфекциям с
летальным исходом (см. раздел «Побочное действие»). Подобные случаи
включают реактивацию латентной вирусной инфекции, например, гепатита В
или C, или инфекции, вызванной полиомавирусами. Сообщалось о случаях
развития гепатита вследствие реактивации вирусов гепатита В или C у
больных-носителей вирусов гепатита В или C, получавших
иммуносупрессивную терапию. Случаи развития ПМЛ, ассоциированные с
JC-вирусом, иногда фатальные, наблюдались у пациентов, принимавших
Селлсепт®.
В сообщениях об этих случаях имеется информация о наличии у пациентов
дополнительных факторов риска развития ПМЛ, включающих
иммуносупрессивную терапию и ухудшение состояния иммунитета. У пациентов
с иммуносупрессией при наличии неврологических симптомов следует
провести дифференциальную диагностику ПМЛ и рекомендовать консультации
невролога.
У пациентов, перенесших трансплантацию почки и принимавших Селлсепт®, наблюдались случаи развития нефропатии, ассоциированной с BK-вирусом (BK virus - associated nephropathy). Данная инфекция может приводить к серьезным последствиям, иногда к гибели трансплантата почки. Следует проводить мониторинг состояния пациентов, принимающих ММФ, для выявления больных с риском развития нефропатии, ассоциированной с BK-вирусом. При развитии симптомов нефропатии, ассоциированной с BK-вирусом, необходимо рассмотреть вопрос о снижении иммуносупрессии.
Система крови и иммунная система
Случаи развития ПККА наблюдались у пациентов, принимавших Селлсепт® в комбинации с другими иммуносупрессивными препаратами. Механизм развития ПККА при применении препарата Селлсепт®не
известен, равно как и вклад других иммуносупрессантов и их комбинации. В
некоторых случаях ПККА была обратимой после снижения дозы препарата
Селлсепт® или отмены. Однако, у пациентов, перенесших трансплантацию, снижение иммуносупрессии может поставить под угрозу трансплантат.
Пациенты, получающие ММФ, должны быть проинформированы о необходимости сразу же сообщать врачу о любых признаках инфекции, кровоточивости, кровотечений или других признаках угнетения костного мозга.
При лечении ММФ необходимо определять развернутую формулу крови в течение первого месяца еженедельно, в течение второго и третьего месяцев лечения - два раза в месяц, а затем на протяжении первого года - ежемесячно. Особое внимание следует обратить на возможность развития нейтропении. Нейтропения может быть связана как с приемом ММФ, так и с применением других лекарственных препаратов, вирусными инфекциями или сочетанием этих причин (см. раздел «Дозирование в особых случаях»). При возникновении нейтропении (абсолютное число нейтрофилов <1.3х103/мкл) необходимо прервать лечение ММФ или уменьшить дозу, при этом проводя тщательное наблюдение за этими пациентами.
В ходе лечения ММФ вакцинация может быть менее эффективной; необходимо избегать применения живых ослабленных вакцин (см. раздел «Взаимодействие с другими лекарственными средствами»). Можно проводить противогриппозную вакцинацию в соответствии с национальными рекомендациями.
Желудочно-кишечный тракт
Прием
ММФ может сопровождаться побочными реакциями со стороны
желудочно-кишечного тракта (изъязвление слизистой оболочки ЖКТ,
желудочно-кишечные кровотечения, перфорации ЖКТ). Необходимо соблюдать
осторожность при применении ММФ у пациентов с заболеваниями
пищеварительного тракта в стадии обострения.
ММФ является ингибитором ИМФДГ, поэтому с теоретической точки зрения, не следует применять его у пациентов с редким генетически обусловленным наследственным дефицитом гипоксантингуанинфосфорибозилтрансферазы (синдромы Леша-Найена и Келли-Зигмиллера).
Взаимодействие
Необходимо
соблюдать осторожность при переходе с комбинированной терапии,
включающей иммуносупрессанты, обладающие влиянием на печеночно-кишечную
рециркуляцию МФК, (например, циклоспорин), на терапию препаратами,
лишенными данного эффекта, (например, сиролимус и белатацепт) и
наоборот. Данный переход может привести к изменению экспозиции МФК.
Необходимо соблюдать осторожность при одновременном применении
препаратов, оказывающих влияние на печеночно-кишечный цикл МФК,
(например, колестирамин, антибиотики) вследствие их способности понижать
плазменную концентрацию и эффективность препарата Селлсепт®.
Отношение риска и пользы одновременного применения ММФ и такролимуса или сиролимуса не установлено. ММФ не рекомендуется применять одновременно с азатиоприном, поскольку оба препарата угнетают костный мозг, и их одновременный прием не изучался.
Особые группы пациентов
Препарат Селлсепт® противопоказан во время беременности и в период грудного вскармливания.
У больных с тяжелой хронической почечной недостаточностью следует избегать применения доз более 1 г 2 раза в сутки (см. разделы «Фармакокинетика в особых клинических случаях» и «Дозирование в особых случаях»).
Коррекция дозы больным с задержкой функции почечного трансплантата не требуется, однако их нужно тщательно наблюдать (см. разделы «Фармакокинетика в особых клинических случаях» и «Дозирование в особых случаях»). Данные по больным, перенесшим пересадку сердца или печени и имеющим тяжелую почечную недостаточность, отсутствуют.
У больных старческого возраста риск нежелательных явлений может быть выше, чем у более молодых пациентов (см. раздел «Побочное действие»).
Обращение с препаратом
Поскольку
ММФ в эксперименте на крысах и кроликах проявил тератогенное действие,
не следует нарушать целостность капсул препарата Селлсепт®. Необходимо избегать вдыхания порошка, содержащегося в капсулах препарата Селлсепт®,
или его прямого попадания на кожу или слизистые оболочки. Если это
произошло, нужно тщательно промыть данный участок водой с мылом, а глаза
- просто водой.
Влияние на способность управлять транспортными средствами, механизмами
При
управлении транспортными средствами, работе с машинами и занятии
другими потенциально опасными видами деятельности необходимо учитывать,
что препарат может вызывать головокружение и другие побочные эффекты,
которые могут влиять на концентрацию внимания и быстроту психомоторных
реакций. При появлении описанных нежелательных явлений следует
воздержаться от выполнения указанных видов деятельности.
Форма выпуска и упаковка
Капсулы 250 мг
По 10 капсул в блистер из пленки поливинилхлоридной и фольги алюминиевой.
10 блистеров вместе с инструкцией по применению помещают в картонную пачку.
Срок годности
3 года. Не использовать по истечении срока годности, указанного на упаковке.
Условия хранения
Хранить при температуре не выше 30°С в оригинальной упаковке для защиты от влаги.
Хранить в недоступном для детей месте.
Условия отпуска из аптек
По рецепту.
Ф. Хоффманн-Ля Рош Лтд., Швейцария
Другие препараты из группы Иммуномодуляторы